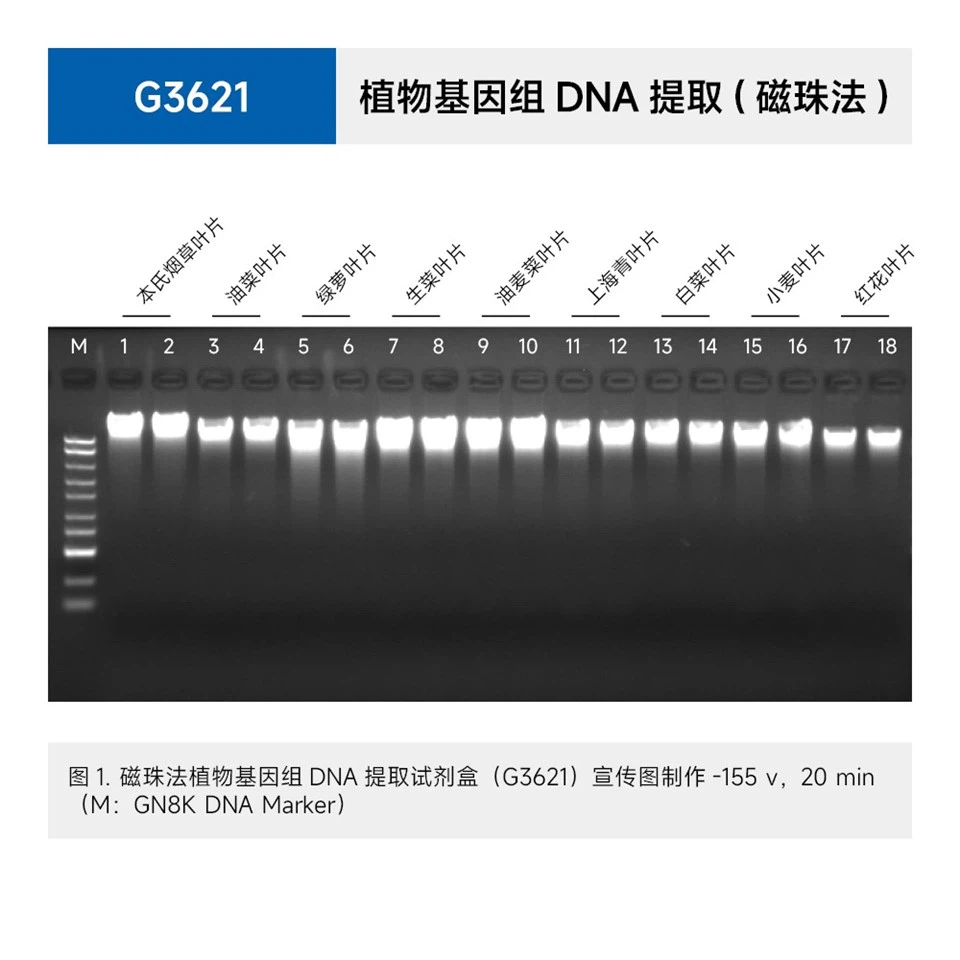
Produktintroduktion
|
Produktnavn |
Kat.nr. |
Spec. |
|
MagBind Plant Genomic DNA Extraction Kit |
G3621-50T |
50T |
Beskrivelse/Introduktion
Ved at bruge superparamagnetiske magnetiske perler, der er specielt udviklet til nukleinsyreekstraktion og -rensning og et specielt optimeret lyseringsbuffersystem, kan dette sæt sikkert, hurtigt og effektivt ekstrahere genomisk DNA med høj renhed fra 50-100 mg plantevævsprøver (såsom hvede, majsblade, osv.). Plantevæv kan hurtigt frigive genomisk DNA efter lysis og effektivt fjerne urenheder undtagen nukleinsyre i prøven. Dette sæt kræver ikke phenol, chloroform og andre organiske reagenser og kræver ikke flertrinscentrifugering. Det ekstraherede genomiske DNA kan anvendes i efterfølgende PCR-reaktion, enzymfordøjelsesreaktion, Southern-hybridisering, RAPD, AFLP, RFLP og mange konventionelle molekylærbiologiske eksperimenter.
Opbevarings- og håndteringsforhold
RNase A sendes med våd is og opbevares ved -20 grad; De resterende reagenser sendes og opbevares ved stuetemperatur; Udløbsdatoen er 12 måneder.
Produktindhold
|
Komponentnummer |
Komponent |
G3621-50T |
|
G3621-1 |
Buffer PGL1 |
30 ml |
|
G3621-2 |
Buffer PGL2 |
5 ml |
|
G3621-3 |
Buffer GB |
30 ml |
|
G3621-4 |
Buffer GD |
16 ml |
|
G3621-5 |
Buffer PW |
24 ml |
|
G3621-6 |
SweMag perler |
2×1 ml |
|
G3621-7 |
RNase A |
1 ml |
|
G3621-8 |
Buffer TE |
10 ml |
|
Manuel |
Ét eksemplar |
|
Før du starter (læs venligst omhyggeligt)
1. Hvis buffer PGL1 udfælder, bedes du opvarme den til 65 grader og bruge den, når den er genoprettet til stuetemperatur.
2. Før brug, tilsæt venligst 24 ml vandfri ethanol til buffer GD og 56 ml vandfri ethanol til buffer PW, bland godt og brug.
3. Selvforsynet magnetisk stativ.
Analyseprotokol/procedurer
1. Lysering af plantevævsprøver:
en. Lysat + Kværn Slibekevner: (anbefalet) Tilføj 50{{10}} μL buffer PGL1 til et 2,0 mL nukleasefrit sliberør (anbefalet HT-200-M) på forhånd , og tilføj derefter 3-4 4 mm rustfri stålperler (anbefalet G0104-200G). Overfør derefter hurtigt 50-100 mg frisk eller kryokonserveret plantevæv til malerøret (bladprøver skæres til 0,5 cm2, rødder og stængler skæres til 0,5 cm). Anbring sliberøret på kværnen (anbefalet KZ-5F-3D) og slib (anbefalet slibeprocedure: indstil frekvensen til 70 HZ, slib i 30 sekunder hver gang, gentag processen {{19 }} gange med 5 sekunders interval mellem hver slibning. Hvis prøven er svær at slibe, såsom rødder og stilke, kan du øge slibningstiderne til 30 eller mere), indtil formalingen er homogeniseret (hvis vævet ikke er grundigt homogeniseret, vil det påvirke udbyttet og kvaliteten af DNA). Efter fuld formaling tilsættes 20 μL RNase A til malerøret, blandes på hovedet og inkuberes ved 65 grader i 15 min., blandes på hovedet hvert 5. minut.
b. Flydende nitrogen + kværn Sliberevner: Overfør hurtigt 50-100 mg frisk eller kryokonserveret plantevæv til et 2,0 mL nukleasefrit malerør (anbefalet HT-200-M, bladprøver skæres til 0,5 cm2, rødder og stængler skæres til 0,5 cm) indeholdende 3~4 3 mm zirconia perler (anbefalet G0203-150G) og forkølet med flydende nitrogen. Anbring sliberøret på kværnen (anbefalet KZ-5F-3D) (afkøl hurtigt adapteren i flydende nitrogen, før du placerer sliberøret), og mal indtil det er fuldstændigt pulveriseret (hvis vævet ikke er fuldstændigt formalet til pulver, vil det påvirke udbyttet og kvaliteten af DNA). Tilsæt derefter 500 μL buffer PGL1 og bland godt, tilsæt 20 μL RNase A til malerøret, bland på hovedet og inkubér ved 65 grader i 15 minutter, bland på hovedet hvert 5. minut.
c. Flydende nitrogen + mørtelslibningsrevner: Overfør hurtigt 50-100 mg frisk eller kryokonserveret plantevæv til en mørtel forkølet med flydende nitrogen (bladprøver skæres til 0,5 cm2, rødder og stængler skæres til 0,5 cm). Tilsæt flydende nitrogen og mal vævet med en støder, tilsæt flydende nitrogen kontinuerligt, indtil det er fuldstændigt pulveriseret (hvis vævet ikke er fuldstændigt formalet til pulver, vil det påvirke udbyttet og kvaliteten af DNA). Overfør derefter de pulveriserede prøver til et 1,5 mL Nuclease-frit centrifugerør indeholdende 500 μL Buffer PGL1 og bland godt. Og tilsæt 20 μL RNase A til centrifugerøret, bland på hovedet og inkuber ved 65 grader i 15 minutter, bland på hovedet hvert 5. minut.
d. Flydende nitrogen + stødstift Kværnende revner: Overfør hurtigt 50-100 mg frisk eller kryokonserveret plantevæv til et 1,5 mL nukleasefrit centrifugerør forkølet med flydende nitrogen (bladprøver skæres til 0,5 cm2 , rødder og stængler skæres til 0,5 cm). Tilsæt flydende nitrogen og kværn vævet med en støder, tilsæt flydende nitrogen kontinuerligt, indtil det er fuldstændigt pulveriseret (hvis vævet ikke er fuldstændigt malet til pulver, vil det påvirke udbyttet og kvaliteten af DNA). Tilsæt derefter 500 μL buffer PGL1 til centrifugerøret og bland godt. Og tilsæt 20 μL RNase A til centrifugerøret, bland på hovedet og inkuber ved 65 grader i 15 minutter, bland på hovedet hvert 5. minut.
2. Tilsæt 100 μL buffer PGL2 til centrifugerøret, bland godt og anbring på is i 5 min.
3. Centrifuger ved 12,000 rpm i 5 minutter ved 4 grader, overfør supernatanten til et nyt 2,0 mL nukleasefrit centrifugerør (hvis der stadig er flydende stof i den opnåede supernatant, det er nødvendigt at centrifugere ved 12,000 rpm i 5 minutter ved 4 grader igen og overføre supernatanten til en anden ny 2.0 mL Nukleasefrit centrifugerør, bemærk: den opnåede supernatant bør ikke overstige 500 μL).
4. Tilføj Buffer GB af samme mængde supernatantvæskevolumen til supernatanten fra det foregående trin, og vend det helt på hovedet og bland godt.
5. Tilsæt den samme mængde isopropanol til blandingen fra det foregående trin, helt på hovedet og bland godt. Tilsæt derefter 40 μL SweMag Beads (SweMag Beads skal være jævnt fordelt før brug) og bland godt med pipette eller vortex-oscillation.
6. Stil ved stuetemperatur i 10 minutter, og under placeringsprocessen, brug pipetten til at blæse eller vortex til at blande flere gange for at holde SweMag Beads i suspension.
7. Overfør centrifugerøret til det magnetiske stativ, og lad det stå i 30 s. Når supernatanten er klar, aspirer og kasser supernatanten.
8. Tilføj 600 μL Buffer GD, fjern det magnetiske stativ, brug en pipette til at blæse eller vortex, indtil SweMag Beads er godt spredt. Overfør centrifugerøret til det magnetiske stativ, og lad det stå i 30 s. Når supernatanten er klar, aspirer og kasser supernatanten.
9. Tilføj 700 μL Buffer PW, fjern det magnetiske stativ, brug en pipette til at blæse eller vortex, indtil SweMag Beads er godt spredt. Overfør centrifugerøret til det magnetiske stativ, og lad det stå i 30 s. Når supernatanten er klar, aspirer og kasser supernatanten.
10. Gentag trin 9.
11. Åbn hætten på centrifugerøret og lad det stå ved stuetemperatur i 5-10 min, så den resterende ethanol kan fordampes fuldstændigt (undgå overtørring af SweMag Beads, hvilket kan påvirke nukleinsyreudbyttet).
12. Fjern det magnetiske stativ, tilsæt 80-100 μL buffer TE eller nukleasefrit vand til centrifugerøret, brug en pipette til forsigtigt at blæse eller vortex, indtil SweMag Beads er godt spredt. Stil ved stuetemperatur i 5 min.
13. Overfør centrifugerøret til det magnetiske stativ, indtil SweMag Beads var fuldstændigt adsorberet, og absorber supernatanten i et nyt 1,5 mL Nuclease-frit centrifugerør for at opnå DNA med høj renhed.
Note
1. Læs venligst produktmanualen omhyggeligt før brug.
2. Prøv at bruge frisk plantevæv for at sikre udbyttet og integriteten af genomisk DNA.
3. De kryokonserverede planteprøver bør undgå gentagen frysning og optøning, ellers vil kvaliteten og udbyttet af ekstraheret DNA blive reduceret.
4. For plantevæv med højt nukleinsyreindhold kan den indledende mængde af plantevævsprøver reduceres passende for at gøre det fuldstændigt lyseret; for prøver med lavt nukleinsyreindhold kan den indledende mængde af plantevævsprøver øges passende for at opnå en højere koncentration af genomisk DNA.
5. Undgå at fryse suspensioner af magnetiske perler under opbevaring. Magnetiske perler er lette at sætte sig, og bør være helt vortex før brug for at holde dem i ensartet suspension.
6. Før du tilføjer magnetiske perler til prøven, skal reagenserne i prøven blandes godt.
7. Ethanol bør fordampes fuldstændigt før eluering af DNA for at undgå påvirkning af resterende ethanol på nedstrøms eksperimenter.
8. Tør ikke magnetiske perler i lang tid for at undgå at påvirke DNA-elueringseffektiviteten.
Skema
Det genomiske DNA-udbytte ekstraheret fra mange simple planteprøver med dette kit er vist i tabellen nedenfor. Genomisk DNA-udbytte er relateret til plantearter, organer og vækststatus. Følgende tabel er kun til reference.
|
Eksempelnavn |
Prøvestørrelse |
DNA-udbytte |
|
Triticum aestivum blad |
50 mg |
25-30 ug |
|
Nicotiana benthamiana blad |
80 mg |
7-10 ug |
|
Carthamus tinctorius blad |
100 mg |
2-5 ug |
|
Brassica napus blad |
100 mg |
5-10 ug |
|
Epipremnum aureum blad |
100 mg |
5-8 ug |
|
Lactuca sativa L. var. ramosa blad |
100 mg |
55-65 ug |
|
Lactuca sativa blad |
100 mg |
35-40 ug |
|
Brassica chinensis blad |
100 mg |
30-35 ug |
|
Brassica pekinensis blad |
100 mg |
20-25 ug |
Kun til forskningsbrug!
Populære tags: magbind plante genomisk dna ekstraktionssæt, Kina magbind plante genomisk dna ekstraktionssæt producenter, leverandører, fabrik